Série (4/6) « Inspiré par la nature »
Nonchalante, l’étoile de mer se meut en collant et décollant sur le substrat marin les minuscules pieds ambulacraires qui tapissent la face postérieure de ses bras. A chaque pas, elle laisse derrière elle une empreinte de colle.
Capable d’adhérence en milieu aqueux et salin, sur tout type de substrat et tissu, cette colle représente le Graal pour des applications médicales. Par exemple, en vue d’arrêter une hémorragie ou de recoller des membranes délicates à l’aide d’un patch adhésif à la colle bioinspirée.

Un travail de longue haleine
Voilà 20 ans que le Laboratoire de Biologie des Organismes Marins et du Biomimétisme (BOMB) de l’Université de Mons caractérise patiemment, au gré des financements, la colle d’une espèce d’étoile de mer. En parallèle, une méthode douce, adoptant des principes de la chimie verte tels qu’énoncés par l’UNESCO, a été développée pour synthétiser les protéines adhésives de ce bio-matériaux.
La marche de l’étoile de mer © Patrick Flammang / Université de Mons
Cette bio-inspiration jusqu’aux paillasses des chimistes suscite l’espoir d’une transition chimique globale dans les process industriels. C’est-à-dire l’abandon du « heat, beat and treat », nom du cocktail démoniaque de la technosphère. Il caractérise les traitements thermiques, mécaniques et chimiques lourds desquels sont issus la plupart des matériaux manufacturés.
Focus sur la protéine adhésive la plus abondante
« Quand on pense à un adhésif, on imagine souvent une substance homogène. Mais dans la nature, la plupart des adhésifs sont hétérogènes, constitués de plusieurs molécules qui ont chacune une fonction bien définie », explique Dr Patrick Flammang, directeur de recherches du FNRS au sein du laboratoire BOMB.
L’empreinte de colle laissée par l’étoile de mer héberge pas moins de 30 protéines. C’est énorme, en particulier quand on envisage de synthétiser le mélange. En investiguant l’endroit de production de chacune de ces protéines, les chercheurs ont découvert qu’une dizaine d’entre-elles n’étaient pas excrétées par des cellules adhésives mais étaient des artefacts provenant de tissus de pied ambulacraire. Voilà qui a allégé la composition de la colle à 20 protéines.
C’est sur la plus abondante d’entre elles que les efforts se sont concentrés. Aujourd’hui, grâce notamment à un projet ARC (Action de Recherche Concertée), cette molécule géante est totalement caractérisée. « Sa séquence d’acides aminés est connue complètement ainsi que certaines caractéristiques chimiques. On a ainsi pu montrer qu’elle avait des sous-unités connues dans la littérature scientifique pour leur rôle dans l’adhérence de protéines », poursuit Dr Flammang.
Méthode des protéines recombinantes
Maintenant que l’on connaît son visage… Et si on la copiait ? Dans le cadre de son doctorat, Elise Hennebert a développé une méthode capable de synthétiser cette protéine adhésive à température et pression ambiantes et sans autre solvant que l’eau, comme cela se fait dans la nature. Elle en dévoile les premiers éléments :
Un plasmide, c’est un petit bout d’ADN circulaire. La méthode consiste à lui greffer l’ADN codant pour la protéine choisie. De la sorte, la bactérie abritant ce plasmide se met à synthétiser la protéine en question, en plus d’autres protéines pour son fonctionnement propre.
Mais dans cette soupe protéique, comment récupérer celle aux propriétés adhésives ?
« On a recours au génie génétique afin qu’elle soit produite en fusion avec une petite étiquette. Celle-ci est composée de 6 acides aminés appelés histidines, placés à la queue leu leu juste à la suite de notre protéine d’intérêt, explique Dr Elise Hennebert, qui est désormais première assistante au laboratoire de biologie cellulaire (UMons). Ensuite, on utilise de la chromatographie dont les colonnes d’affinité sont composées de microbilles de sepharose contenant du nickel. Lorsque l’on fait couler le mélange de protéines produites par les bactéries, ce dernier attire l’histidine qui se colle alors aux billes, entraînant avec elle la protéine d’intérêt. Il ne reste plus qu’à laver pour la récupérer. »
Cette méthode utilisant un plasmide commercial contenant de l’ADN codant pour les 6 histidines de l’étiquette est désormais utilisée à large échelle. Elle permet de produire biologiquement des protéines d’intérêt sans avoir recours à la synthèse chimique. A défaut de présenter une empreinte environnementale nulle, elle s’approche néanmoins des procédés de chimie verte. C’est un premier pas dans la direction biomimétique.
Les matériaux du vivant construits à partir d’une sélection réduite d’atomes
L’enjeu du biomimétisme dans le secteur des matériaux est de parvenir à sortir d’une logique d’économie linéaire, gourmande en énergie ainsi qu’en ressources, et reposant sur des matières premières rares, difficiles à extraire et à purifier. Nous allons, dans la suite de cet article, débroussailler quelques-uns des principes du vivant , étoile polaire des biomiméticiens.
Tout d’abord, le vivant est façonné au départ d’une vingtaine d’éléments atomiques parmi les plus courants sur Terre. Six d’entre eux façonnent plus de 96% de la matière vivante. Ils sont connus sous l’acronyme CHONSP (carbone, hydrogène, oxygène, azote, souffre, phosphore).
Cette économie d’atomes n’empêche pas une riche diversité de biomatériaux. Il y a les céramiques, à base de sels de calcium et de silice. Mais aussi les biopolymères, dont font partie les protéines (comme celles de la colle d’étoile de mer ou d’autres exerçant une fonction de catalyse enzymatique, d’hormones, d’anticorps, etc. ) ainsi que les polysaccharides (glucides) et les acides nucléiques (composants de l’ADN).
Par ailleurs, le vivant utilise un large panel de biomatériaux composites. Ils ont la particularité d’être constitués d’une alternance de phases dures d’origine minérale ou cristalline et de phases molles organiques ou amorphes davantage résistantes à la rupture. C’est le cas des os, des carapaces, du byssus de moule, du bois, mais aussi de la soie d’araignée.
Cette dernière est en effet un matériau composite de protéines façonné de 20 % de cristaux dans une matrice amorphe. A l’état liquide dans le corps de l’animal, la soie se déshydrate juste avant son excrétion et se solidifie en fibres lors de son extrusion à l’air libre. Parmi les 47.000 espèces d’araignées recensées à ce jour, la plupart produisent un type de fibres de soie unique. La championne de la toile d’araignée alliant la plus grande élasticité à un maximum de résistance à la traction est une arachnide malgache répondant au nom Caerostris Darwini. Par rapport au Kevlar, ses fibres de soie peuvent supporter une quantité d’énergie 10 fois supérieure avant de rompre. Et cela, au départ d’une base de quelques atomes savamment agencés en conditions ambiantes.
La nature, pionnière du zéro déchet
De la base atomique commune CHONSP découle un avantage hors-norme : la recyclabilité totale. Toutes les molécules du vivant, qu’elles constituent des organes, des os, des pétales ou des venins, se décomposent, à la fin de leur vie, en briques plus petites. Ces dernières sont alors facilement réutilisées par des individus de la même espèce ou d’une autre espèce pour bâtir de nouveaux bio-matériaux. De cette façon, aucun déchet n’est produit. Le résidu de l’un devenant la matière première d’un autre. C’est ainsi que le biomimétisme pourrait être utilisé comme un outil permettant d’assurer que le développement de nouveaux matériaux s’inscrit bien dans l’économie circulaire.
Ensuite, là où l’humain consomme des montagnes d’énergie pour chauffer et pressuriser un mélange afin de lier des atomes récalcitrants en une association contre nature, le vivant fait sa chimie à pression et température ambiantes. Ses matériaux aux formes folles, à l’organisation multi-échelle et parfois à la résistance inégalée, il les conçoit par autoassemblage et croissance adaptative dans l’eau de ses cellules (un humain est constitué à 65% d’eau, une méduse à 98%), sans avoir recours au moindre solvant toxique.
Un rêve d’ingénieur : une structure d’aile, trois fonctions physiques
Pourquoi limiter un matériau à une seule fonction ? Au contraire de l’humain qui conçoit ses matériaux pour répondre à un unique besoin, la nature opte pour la multifonctionnalité.
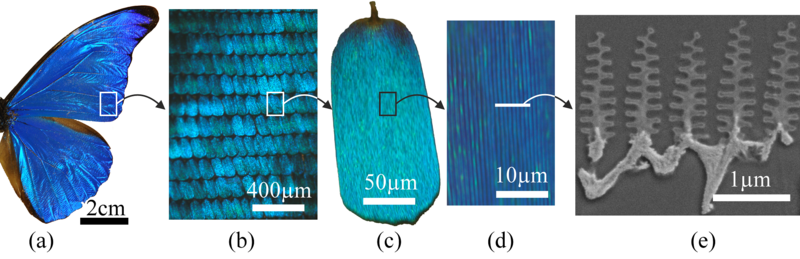
Prenons l’exemple de l’aile du morpho, une espèce de papillon sud-américain. Sa structure multi-échelle se divise en plusieurs niveaux : l’aile (qui fait quelques centimètres) est recouverte d’écailles (de l’ordre d’une centaine de microns), lesquelles sont parcourues par des stries (µm), elles-mêmes portant des lamelles équidistantes de l’ordre d’une centaine de nm. En leur cœur, de la chitine et de la mélanine (d’une taille avoisinant les 0,3 nm). Cette structure complexe est construite au départ d’une poignée d’atomes CHONSP et remplit des fonctions mécaniques, optiques et thermiques.
En effet, l’aile de morpho est tellement hydrophobe qu’elle en est autonettoyante. Sa structure nanométrique, en diffractant certaines longueurs d’onde de lumière, lui confère sa splendide couleur bleu si caractéristique. Il n’y a donc pas le moindre pigment bleu dans l’aile du morpho. Enfin, cette dernière régule la chaleur de l’animal. En effet, lorsque sa température physique excède 40°C, la chitine des ailes se met à émettre dans l’infrarouge afin de faire chuter sa température. Autant de fonctions physiques regroupées en une seule structure, c’est véritablement un rêve d’ingénieur.
Une transition chimique en deux temps ?
Mais, « très souvent, on ne sait pas encore fabriquer des matériaux aussi sophistiqués que le vivant. Il est impossible d’imiter les structures naturelles hiérarchisées à de multiples échelles avec nos méthodes traditionnelles de manufacture. Pour y arriver, il faut que nos procédés industriels changent drastiquement », insiste Kalina Raskin, directrice générale du Centre Européen d’Excellence en Biomimétisme de Senlis (CEEBIOS). Selon elle, les avancées dans différents domaines scientifiques et techniques pourraient contribuer à la réussite de ce challenge :
Cette transition dans la manière de faire de la chimie et de concevoir des matériaux ne se fera vraisemblablement que graduellement. D’abord de façon bio-inspirée, où l’on ne copiera que quelques éléments des procédés naturels de fabrication pour parvenir, peut-être, à terme, à les imiter totalement. Et de la sorte, à réduire drastiquement notre impact délétère sur l’environnement.
Cette enquête a bénéficié du soutien du Fonds pour le journalisme en Fédération Wallonie-Bruxelles

