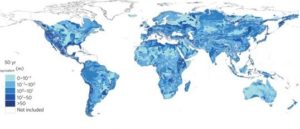
Comment retarder l’emballement climatique ? Une solution potentielle serait d’injecter dans des nappes phréatiques le CO2 atmosphérique excédentaire capté localement. Certaines nappes sont, en effet, si salées qu’elles ne sont utilisables ni pour l’eau potable ni pour l’agriculture. Et, point intéressant, on en trouve tout autour du globe.
Mais avant de généraliser un tel procédé, il faut prédire les risques, en calculer l’efficacité et évaluer le devenir à long terme du CO2 emprisonné. Ces aspects requièrent une compréhension détaillée des dynamiques physico-chimiques et du transport des espèces chimiques dans les sous-sols.
Expérimentation au labo
À l’ULB, utilisant de petits réacteurs, des chimistes expérimentent la séquestration du CO2 dans les aquifères. Dans de l’eau, plus ou moins chargée en composés chimiques, ils injectent le gaz à effet de serre. Le système créé au laboratoire est simplifié, car n’y sont simulées ni la température ni les dantesques conditions de pression qui règnent dans les tréfonds de la Terre par 800 ou 1000 m de profondeur. C’est-à-dire là où se trouvent les aquifères qui pourraient devenir l’hôte final du surplus de CO2 atmosphérique.
« Au niveau quantitatif, les résultats générés avec ce système ne sont pas ceux qu’on obtiendrait en conditions réelles. Néanmoins, on essaie de démontrer que les taux de transfert du CO2 vers la phase hôte sont différents selon qu’il y ait ou non des réactions chimiques », explique Pre Anne De Wit, directrice de l’Unité de Chimie Physique Non Linéaire. « Cette réactivité chimique peut fortement amplifier le taux de transfert. » Et donc le taux de séquestration du CO2.
Un aquifère n’est pas l’autre
La quantité de CO2 qui pourrait être absorbée dépend directement de la composition chimique de l’eau d’un aquifère particulier.
Cette subtilité, les rapports du GIEC ne la prennent pas en compte. Or, « si, comme le suggère le GIEC, cette méthode doit un jour être envisagée pour réaliser une transition vers une société sans carbone, il faut être capable de prédire le nombre de mégatonnes de CO2 qui pourraient être séquestrées par ces techniques. Actuellement, ces prédictions se basent sur des modélisations. Mais pour avoir confiance en elles, et à défaut d’aller contrôler ce qu’il se passe à 1000 mètres de profondeur avec des monitorings complexes, il faut tester les prédictions de ces modèles sur des expériences que l’on contrôle. C’est ce que nous faisons dans les réacteurs au laboratoire. Les résultats obtenus peuvent ensuite être extrapolés suivant les conditions du terrain et utilisés pour prédire le taux de CO2 que ces techniques pourront effectivement stocker. Et ce, en ayant davantage confiance dans les modèles. »
Minéralisation du CO2
Un objectif majeur de la séquestration du CO2 est sa minéralisation. C’est-à-dire la transformation de ce gaz à effet de serre en minéraux inoffensifs grâce à des réactions de précipitation.
La dissolution du CO2 dans l’eau produit des ions carbonates. Chargés deux fois négativement, ils se lient facilement aux ions magnésium et calcium, chargés quant à eux deux fois positivement, et forment des précipités. C’est, par exemple, le calcaire qui se dépose sur nos éviers.
« D’autres réactions pourraient avoir lieu quand le CO2 va se dissoudre dans les aquifères salins. S’il réagit avec des ions pour former un précipité qui va couler dans le fond, c’est très prometteur. Car alors le CO2 est stocké sous forme solide, et non plus sous forme de gaz qui risquerait d’être relargué vers l’atmosphère lors d’un tremblement de terre par exemple. On dit que le CO2 est minéralisé. C’est plus sécurisant pour le stockage. »
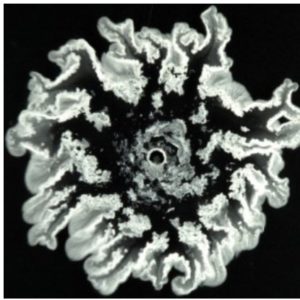
Grâce à des expériences modèles réalisées en laboratoire, l’équipe de la Pre De Wit tente de définir les conditions optimales de minéralisation du CO2 en fonction des concentrations et de la vitesse d’injection.
Des premiers tests grandeur nature en Islande et en mer du Nord
Ces informations pourront aiguiller nos dirigeants à choisir, en fonction des roches qui les composent, les nappes aquifères les plus adéquates à la séquestration du CO2.
Ces méthodes de séquestration pourraient-elles être utilisées à grande échelle d’ici peu ? « Je pense que oui, poursuit la Pre De Wit. Récemment, des tests ont été faits dans des sites en Islande et dans la mer du Nord. Ils ont montré qu’on pouvait y stocker des mégatonnes de CO2. En Islande, le CO2 a été injecté dans des roches basaltiques, très riches en réactifs, dont des ions calcium et magnésium : très rapidement, en moins de deux ans, une grande partie du CO2 a bien été stockée. C’est très prometteur. Mais il y a un souci : actuellement, la technique coûte très cher. Qui va payer ? »
Pour l’heure, en mer du Nord, ce sont les sociétés pétrolières qui sont en à la manœuvre, en essayant de faire d’une pierre deux coups : injecter du CO2 dans les gisements pour faciliter l’extraction du … pétrole, puissant fournisseur de gaz à effet de serre.

